el carbono es un elemento único en la naturaleza ya que, sus propiedades, como sus usos, son muchas, una des sus propiedades es que es muy poco maleable ya que es muy frágil, por lo que no se pueden formar laminas de carbono, como los no metales, no puede conducir corriente eléctrica, y carece de lustre, otra cosa que lo hace tan especial es el hecho de que pueda compartir hasta 4 electrones, lo que hace que pueda formar cadenas muy largas con los demás elementos o con el mismo elemento, así como el hecho de que cuando forme sus enlaces puedan ser de tipo lineales, cerrados o formen anillos, también es el principal agente en los hidrocarburos y la formación de grafitos y diamantes.
HIDROCARBUROS

los hidrocarburos se pueden entender también como, los enlaces entre hidrógeno y carbono.
FORMULA Y NOMENCLATURA
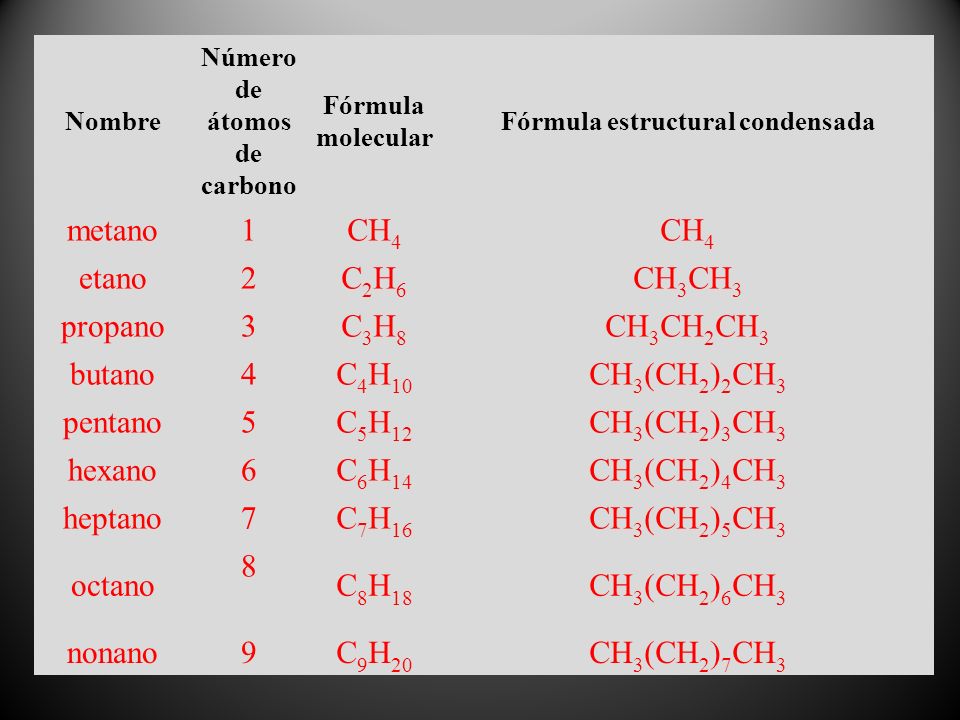
hay varias formas de representar a los hidrocarburos, entre ellas están la formula "desarrollada", la "semi-desarrollada", la de "esqueleto", la de "esferas y palos" y la "condensada".
la formula desarrollada es cuando se representan todos sus átomos de hidrógeno y carbono de manera plena.

la formula semi-desarrollada es cuando se agrupan los hidrógenos al átomo de carbono con el que están enlazados.

e cortas.
la formula de esqueleto son unas lineas en zigzag que en cada vertice representan átomos de carbono no se muestran los atomos de hidrogeno

la formula de esferas y palos es una representacion tridimensional que se hace mediante, como su nombre lo dice con esferas y palos

y la ultima formula, pero no menos importante, la formula condensada se agrupan los átomos, y es útil para ver la composición pero no la estructura
COMPUESTOS DEL CARBONO
gracias a que el carbono tiene gran afinidad eléctrica, se le puede ver con varios elementos, y no solo con el hidrógeno, formando así enlaces con el nitrógeno, azufre, etc..., al combinarse el carbono con el hidrógeno y el nitrógeno se puede obtener vitamina B1.
otras estructuras con el carbono, pueden ser las bases del ADN, como adenina, timina, uracilo, citosina y guanina.
ISOMERIA
un isomero se puede representar mediante la formula condensada, ya que hay enlaces que poseen la misma formula condensada pero tienen diferentes propiedades y estructuras, por ejemplo:

EJERCICIOS
Bibliografía
Libros
Dingrando, L. et al. (2002). Química, Materia y Cambio. Colombia: McGraw- Hill.
García, J. y Ortega, F. (2004). Periodicidad Química. México: Trillas.
Espriella, A. (2011). Química Orgánica Básica. Un acercamiento a la estructura en el nivel nanoscópico para explicar lo macroscópico. México: Universidad Autónoma de México, UAM.
Lewis, M. y Waller, G. (1995). Química Razonada. México: Trillas.
Morrison, R. y Boyd, R. (1998). Química orgánica. México: Ed. Addison Wesley Longman.
García, J. y Ortega, F. (2004). Periodicidad Química. México: Trillas.
Espriella, A. (2011). Química Orgánica Básica. Un acercamiento a la estructura en el nivel nanoscópico para explicar lo macroscópico. México: Universidad Autónoma de México, UAM.
Lewis, M. y Waller, G. (1995). Química Razonada. México: Trillas.
Morrison, R. y Boyd, R. (1998). Química orgánica. México: Ed. Addison Wesley Longman.
Internet
Textos científicos (s/f). Modelo de Repulsión de los Pares de Electrones de la Capa de Valencia. Recuperado de http://www.textoscientificos.com/quimica/inorganica/vserp (abril, 2012).
Videos
El carbono (s/f). Recuperado de http://www.youtube.com/watch?v=365Iq9EYNE0&feature=related (abril, 2012).
Enlace carbono-carbono (s/f) Recuperado de http://www.youtube.com/watch?v=YQ3k_NgvrxI&feature=related (abril, 2012).
Enlace carbono-carbono (s/f) Recuperado de http://www.youtube.com/watch?v=YQ3k_NgvrxI&feature=related (abril, 2012).
Imágenes
Carbón. Recuperado de
http://www.marilolopezgarrido.com/wp-content/uploads/2011/06/Carbon.jpg (abril, 2012)
Carbono amorfo. Recuperado de http://upload.wikimedia.org/wikipedia/commons/thumb/9/90/Amorphous_Carbon.png/220px-Amorphous_Carbon.png
Diamante y grafito. Recuperado de http://3.bp.blogspot.com/-PGf5rzOBpaw/Tp5HJjJwugI/AAAAAAAAAOQ/FLkxz6Dj0Rc/s1600/diamante%2Bcarbon.jpg (abril, 2012).
Metil-propano. Recuperado de
https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEgErCednuvAWDdbEomFFLhlNS1l5ggNstMpVwqqWb_tdiRQLqWclAJ_iWkSlTDNsEe1_uHB1tGr1ntyiw1e2BlOtFTt5cNlDvNYNlUq12QCpr0rSc5y1owjGW2qN23nKFeG7ZR-BQ406Lk/s400/metilpropano.jpg
Metoxienato. Recuperado de http://upload.wikimedia.org/wikipedia/commons/thumb/9/96/Methoxyethane-3D-balls.png/220px-Methoxyethane-3D-balls.png
Nanotubo. Recuperado de
http://www.ecuadorciencia.org/images/nanotecnologia/nanotubo-carbono2.jpg
N-butano. Recuperado de http://wikienergia.com/~edp/images/thumb/3/31/MoleculaNButano.jpg/300px-MoleculaNButano.jpg
1-propanol. Recuperado de
http://www.tennoji-h.oku.ed.jp/tennoji/oka/2004/1-propanol-b.gif
2-propanol. Recuperado de
http://www.tennoji-h.oku.ed.jp/tennoji/oka/2004/2-propanol-b.gif
http://www.marilolopezgarrido.com/wp-content/uploads/2011/06/Carbon.jpg (abril, 2012)
Carbono amorfo. Recuperado de http://upload.wikimedia.org/wikipedia/commons/thumb/9/90/Amorphous_Carbon.png/220px-Amorphous_Carbon.png
Diamante y grafito. Recuperado de http://3.bp.blogspot.com/-PGf5rzOBpaw/Tp5HJjJwugI/AAAAAAAAAOQ/FLkxz6Dj0Rc/s1600/diamante%2Bcarbon.jpg (abril, 2012).
Metil-propano. Recuperado de
https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEgErCednuvAWDdbEomFFLhlNS1l5ggNstMpVwqqWb_tdiRQLqWclAJ_iWkSlTDNsEe1_uHB1tGr1ntyiw1e2BlOtFTt5cNlDvNYNlUq12QCpr0rSc5y1owjGW2qN23nKFeG7ZR-BQ406Lk/s400/metilpropano.jpg
Metoxienato. Recuperado de http://upload.wikimedia.org/wikipedia/commons/thumb/9/96/Methoxyethane-3D-balls.png/220px-Methoxyethane-3D-balls.png
Nanotubo. Recuperado de
http://www.ecuadorciencia.org/images/nanotecnologia/nanotubo-carbono2.jpg
N-butano. Recuperado de http://wikienergia.com/~edp/images/thumb/3/31/MoleculaNButano.jpg/300px-MoleculaNButano.jpg
1-propanol. Recuperado de
http://www.tennoji-h.oku.ed.jp/tennoji/oka/2004/1-propanol-b.gif
2-propanol. Recuperado de
http://www.tennoji-h.oku.ed.jp/tennoji/oka/2004/2-propanol-b.gif








No hay comentarios:
Publicar un comentario